久松理一
松本主之、仲瀬裕志、渡辺憲治、久松理一、本谷聡、蘆田知史、伊藤裕章、鈴木康夫、松本譽之、松井敏幸、日比紀文、渡辺守
研究概要紹介
01 | 目的・試験デザイン
目的
アダリムマブおよびアザチオプリンの併用療法の有効性と安全性を明らかにする。
試験デザイン
多施設共同プロスペクティブランダム比較試験(オープンラベル)。
02 | 試験プロトコール

03 | 対象
対象症例
抗TNFa抗体製剤および免疫調整剤の使用経験がない中等症・重症(CDAI: 220-450)のCD患者。
症例数
200例(各群100例の2群間比較)。アダリムマブ単独群の寛解率を40%、アダリムマブ+アザチオプリン併用群の寛解率を60%と仮定すると検出力80%、aエラー5%で各群95例が必要。
04 | 各群の投与薬剤・方法
投与方法
- アダリムマブ単独群
初回160mg、2週後80mg、以後2週ごとに40mgを継続投与する。 - アダリムマブ+アザチオプリン併用群
上記に加えアザチオプリン25-100mg/日を併用する。
4週後までに投与量を固定し、以後増量は行なわない。ただし、減量は可能。
試験薬剤・併用薬・栄養療法の投与量変更
試験薬剤および試験の結果に影響を与える可能性のある5-ASA製剤および栄養療法は投与量を変更しない。
ステロイドは減量は可であるが、増量は不可とする。
05 | 評価項目
主要評価項目
- 26週後の寛解率
副次評価項目
- 各観察期間での寛解率、CR70、CR100
- 26週後、52週後の粘膜治癒率
- 26週後、52週後のdeep remission (DR) 達成率
DR:CDAIが150未満かつ粘膜治癒が得られているもの - 効果減弱(再燃)率
4週後にCR100の寛解を達成し、その後CDAIが100以上上昇かつ150以上の状態になった場合
(CDAI≥150かつDCDAI≥100) - 有害事象発生率
06 | 臨床検査・内視鏡検査スケジュール
| 投与前 (-2~0週) |
2週 | 4週 | 12週 | 26週 | 52週 | |
|---|---|---|---|---|---|---|
| 患者背景 | ◯ | |||||
| 問診 | ◯ | ◯ | ◯ | ◯ | ◯ | ◯ |
| CDAI | ◯ | ◯ | ◯ | ◯ | ◯ | ◯ |
| 大腸内視鏡 | ◯ | ◯ | ◯ | |||
| 小腸内視鏡 | (◯) | (◯) | (◯) | |||
| 血液検査 | ◯ | ◯ | ◯ | ◯ | ◯ | ◯ |
| 血中濃度抗体測定 | ● | |||||
| 6TGN濃度 | ◯ | |||||
| 有害事象 | 随時確認 | |||||
07 | 26週の血中濃度・抗体測定の注意事項
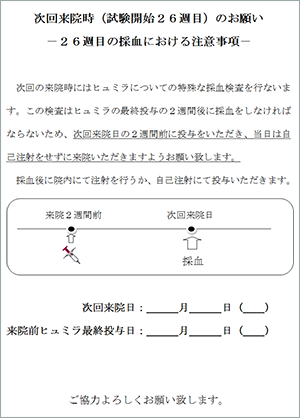
血中濃度・抗体測定はアダリムマブのトラフで測定する必要があります。
測定2週間前に投与いただき当日は投与する前に採血を行う必要があります。
上記についての患者さんへのお願い文書をご用意しましたのでご利用いただき、徹底をお願い致します。
インフォメーション
- 2020.03.31終了しました

